Zelluläre Testsysteme
Forschungsaktivitäten Ercan Herbst-Lab
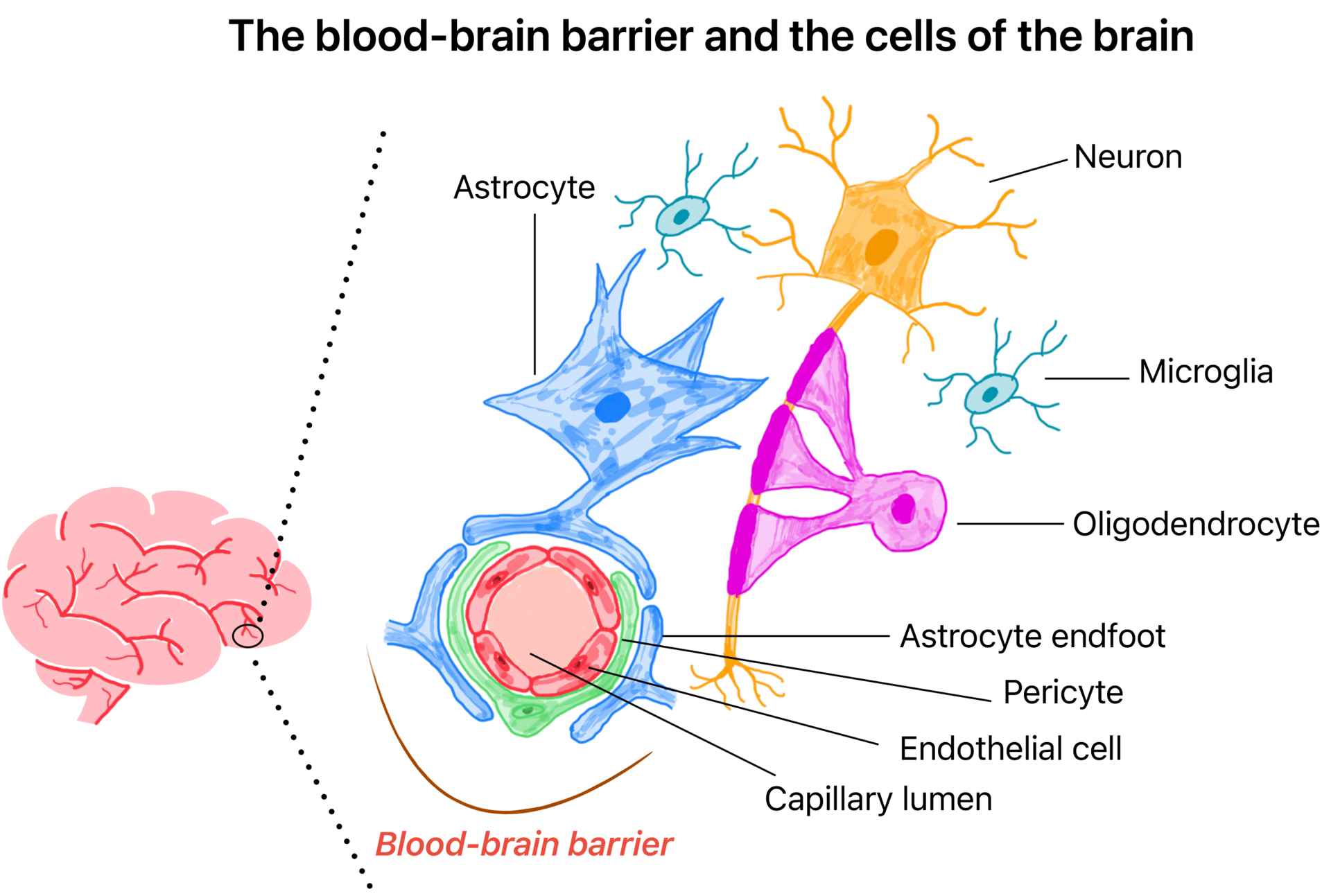


Das aktuelle Forschungsprojekt befasst sich mit der Entwicklung eines fortschrittlichen Modells auf Basis induzierter pluripotenter Stammzellen zur Untersuchung der menschlichen Blut-Hirn-Schranke.
Projekt: 3D-hiPSC-BHS – In-vitro-Plattform auf Basis humaner Stammzellen zur Untersuchung der Blut-Hirn-Schranke, des Wirkstofftransports und neurologischer Erkrankungen
Die Blut-Hirn-Schranke (BHS) ist eine hochselektive Barriere, die das Gehirn vor schädlichen Substanzen im Blutkreislauf schützt und gleichzeitig ein stabiles Umfeld für die neuronale Aktivität gewährleistet. Eine Funktionsstörung der BHS steht im Zusammenhang mit einer Vielzahl neurologischer Erkrankungen. Zugleich stellt ihre Schutzfunktion ein erhebliches Hindernis für die effektive Verabreichung therapeutischer Wirkstoffe an das Gehirn dar. Daher besteht ein dringender Bedarf an physiologisch relevanten, humanbasierten Modellen zur Förderung der neuropharmazeutischen Forschung.
Unter der Leitung von Prof. Dr. Ebru Ercan Herbst wird im Projekt 3D-hiPSC-BHS daran gearbeitet, dieser Herausforderung zu begegnen, indem ein fortschrittliches in-vitro-Modell der Blut-Hirn-Schranke (BHS) auf Basis humaner induzierter pluripotenter Stammzellen (iPS-Zellen) entwickelt wird. Dieses Modell integriert verschiedene Hirnzelltypen in ein nanofaserbasiertes 3D-Gerüst und ein Transwell-System. Es bietet eine vielversprechende Plattform zur Bewertung der Wirkstoffdurchlässigkeit, zur Untersuchung zellulärer Reaktionen und zur Erforschung der molekularen Mechanismen, die zur Schädigung der BHS bei neurodegenerativen und neurologischen Erkrankungen führen.
Projektlaufzeit: 01.01.2025-31.12.2026
Förderung: Carl-Zeiss-Stiftung Forschungsstart Programm
Ansprechpersonen







